César Paz-y-Miño. Investigador en Genética. Universidad UTE, para Notimercio.
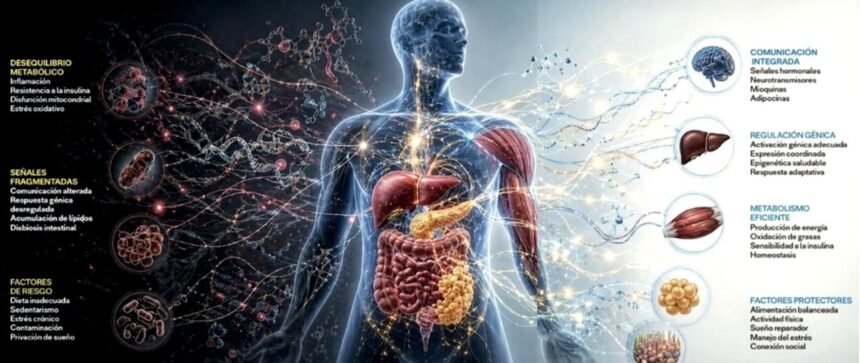
El metabolismo humano funciona como una red integrada donde órganos, señales hormonales y expresión genética interactúan de forma dinámica y constante. Más que procesos aislados, sistemas como el páncreas, hígado, músculo, intestino y tejido adiposo coordinan funciones a través de redes génicas influenciadas por el entorno
El metabolismo humano no es una suma de órganos que funcionan en paralelo; es una red integrada de tejidos que intercambian información de manera constante, a través de señales hormonales, metabolitos y programas genéticos finamente regulados. Esta visión, que hoy se consolida desde la biología de sistemas, rompe con el paradigma clásico de la fisiología fragmentada. El cuerpo no “tiene” metabolismo: es metabolismo. Y ese metabolismo es, en esencia, una estructura genética en acción.
En esta red, cada órgano no solo ejecuta funciones, sino que interpreta y modula señales que terminan reconfigurando la expresión de genes en otros tejidos. El páncreas, regula la secreción de las enzimas insulina y glucagón, modulando rutas metabólicas en hígado, músculo y tejido adiposo. Pero más allá de su función endocrino-hormonal clásica, su influencia es profundamente genómica, es decir, redes de genes: la insulina activa cascadas intracelulares que terminan regulando factores celulares que cumplen órdenes genéticas, determinando si las células del hígado produce glucosa o sintetiza lípidos. Así, una señal hormonal, se convierte en un cambio en la estructura funcional del genoma.
El hígado, actúa como un centro integrador de información metabólica. Recibe señales del sistema nervioso, del tejido adiposo, del intestino y del músculo, y las traduce en respuestas bioquímicas que dependen de la activación o represión de redes génicas específicas. Algunos genes son esenciales para la formación de glucosa en hígado y en los riñones, glucosa no proveniente de carbohidratos, sino de lípidos, que se activan en estados de ayuno, mientras que otros genes, coordinan la degradación de ácidos grasos durante la formación de cuerpos cetocicos (energía sin carbohidratos). Esta regulación no es estática: es dinámica, dependiente del contexto nutricional, hormonal y ambiental. El hígado no decide por si solo; responde a un sistema de señales que constantemente lo están programando, por intermedio de genes especializados, y todo esto en tiempo real.
El músculo esquelético introduce una dimensión adicional en esta red: la del movimiento como modulador genético. Durante la contracción muscular, se activan vías metabólicas que no solo consumen energía, sino que envían señales al resto del organismo. Las mioquinas o proteínas liberadas por el músculo, actúan sobre el tejido adiposo y el hígado, modificando la sensibilidad a la insulina y la producción de glucosa. Igualmente este fenómeno está mediado por genes, que regulan la actividad biológica y funcional de las mitocondrias, que actúan como sensores energéticos celulares. Las mitocondrias son la fábrica de la energía. El ejercicio, en este sentido, no es solo una actividad física: es una intervención directa sobre la regulación de la expresión de los genes en un ambiente determinado, que a su vez, reconfigura la expresión génica sistémica e interactiva.
El intestino, por su parte, representa una interfaz crítica entre el ambiente y el genoma. A través de la microbiota, transforma componentes dietéticos en metabolitos que actúan como moduladores entre genes y ambiente. Los ácidos grasos producidos por las bacterias, por ejemplo, inhiben componentes proteicos del ADN, promoviendo una estructura menos densa del ADN y favoreciendo la generación de sustancias comandadas por genes asociados al equilibrio metabólico y la regulación inmunológica. Además, hormonas intestinales como GLP-1 no solo regulan el apetito y la secreción de insulina, sino que influyen en la expresión génica en tejidos periféricos. Además otros genes integran estas señales, convirtiéndose en nodos críticos donde convergen la genética, la nutrición y el riesgo de enfermedad.
El tejido adiposo completa este circuito como un órgano endocrino activo, cuya función trasciende el almacenamiento de energía. La secreción de adipocinas como leptina, adiponectina y asprosina modula el apetito, la sensibilidad a la insulina y la producción hepática de glucosa. Estas funciones están reguladas por genes específicos, cuyas variantes pueden alterar la comunicación interorgánica. En condiciones de disfunción, el tejido adiposo se convierte en un generador de señales inflamatorias, que perpetúan la resistencia a la insulina y el desequilibrio metabólico.
Desde una perspectiva evolutiva, esta red metabólica refleja adaptaciones a entornos de escasez energética. La capacidad de almacenar grasa, movilizar glucosa y ajustar el metabolismo según la disponibilidad de nutrientes, fue crucial para la supervivencia. Sin embargo, en el contexto contemporáneo de abundancia calórica y sedentarismo, estas mismas adaptaciones se vuelven disfuncionales. La persistente activación de rutas de almacenamiento y producción energética conduce a una sobrecarga metabólica que desborda los mecanismos de regulación genética.
Aquí emerge el concepto central: la enfermedad metabólica no es el resultado de una falla aislada, sino de un desacople en la red. La resistencia a la insulina, la obesidad o el hígado graso no alcohólico, son manifestaciones de una pérdida de sincronía entre órganos que ya no responden de manera coordinada a las señales sistémicas. Este desacople tiene una base genética y ambiental: cambios en la expresión génica inducidos por factores ambientales, dietéticos y sociales que alteran la comunicación interorgánica.
Genes y ambiente, actúan como un puente de comandos. Modificaciones como bloqueo químico del ADN o el efecto en las proteínas asociadas al ADN, permiten que factores externos, dieta, actividad física, microbiota, estrés, reprogramen la expresión génica sin alterar la secuencia del ADN. Este fenómeno explica por qué individuos con predisposición genética, no desarrollan enfermedad en entornos favorables, mientras que otros, sin mutaciones evidentes, pueden enfermar en contextos adversos. El genoma no es un destino fijo, sino un sistema dinámico sensible a su entorno.
Pero este entorno no es neutral. Está profundamente condicionado por factores sociales, económicos y políticos. La disponibilidad de alimentos ultraprocesados, la urbanización, la desigualdad en el acceso a servicios de salud y la exposición a contaminantes configuran un paisaje metabólico, que favorece el desacople de esta red. En este sentido, la enfermedad metabólica es también una expresión de inequidad: una patología que emerge de la interacción entre biología y estructura social. De pobreza versus u opulencia.
La práctica clínica, frente a esta complejidad, debe abandonar el reduccionismo. No es suficiente tratar la hiperglucemia o la dislipidemia como fenómenos aislados. Es necesario comprender las redes subyacentes, identificar los puntos de disrupción y diseñar intervenciones que restauren la coherencia del sistema. Esto implica integrar la genética, el ambiente, la nutrición y el contexto social en un enfoque integrador.
El metabolismo en red nos obliga a replantear nuestra comprensión del cuerpo humano. No somos conjuntos de órganos, somos sistemas interconectados donde la información fluye de manera continua y donde los genes responden a esa información, adaptando la función biológica. La salud emerge de la sincronía de esta red; la enfermedad, de su rotura. Y en ese delicado equilibrio, profundamente genético pero inseparable del entorno, se define no solo nuestra fisiología, sino también nuestra vulnerabilidad como especie.